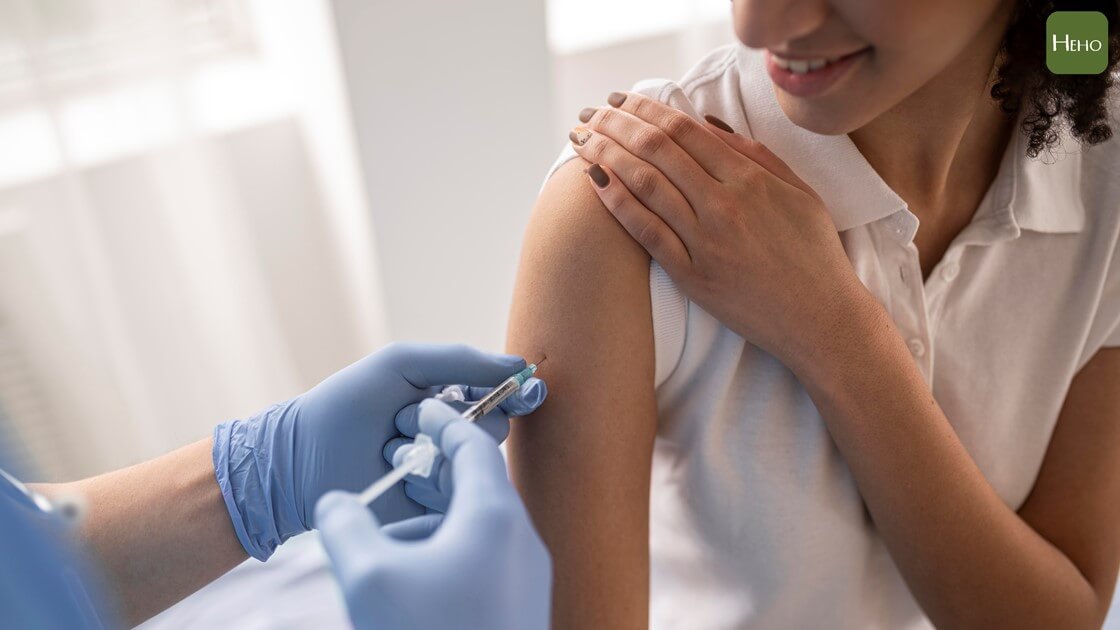
高端疫苗順利通過EUA後,民眾關心接下來什麼時候可以施打,但施打前必須進行量產,但高端送給食藥署審查的批號中卻發現 50L 中有 2 批次抗原稍高,食藥署藥品組林意筑專門委員解釋:「本來製成放大就會有存在差異,但不代表不合格,只是需要去證明分析差異是不影響確效。」
食藥署:高端兩批次發現抗原稍高
食藥署發現高端公司 50 L製程抗原,其中兩批次唾液酸醣修飾化程度較2 L製程抗原稍高、檢驗結果不一樣,必須針對這兩批要求做更近一步檢驗分析是否影響安全,進行製程放大比較測試等作業。
但國產疫苗本來預期在今年暑假就要大量生產製造,時程似乎跟不上規劃,高端順利取得EUA以後可能才是挑戰的開始,因為次蛋白疫苗量產上比起其他製成疫苗更具考驗,製程上可能面臨疫苗不良率的問題,台大藥學系梁碧惠教授解釋:「蛋白質疫苗生產出來會進行很多檢驗,要確保每批次生產的一樣,次蛋白質疫苗本身的控管項目建立比較完整,因此可以說相對安全,但它的問題就是量產和分析相對辛苦!」
次單白疫苗雖安全!量產上容易遇困境
在量產過程中疫苗品質出現問題的情況,其實不只高端有遇到,同樣為次蛋白疫苗的諾瓦瓦克斯(Novavax),即使被認定保護力效果極佳,也面臨量產問題,梁碧惠說:「這樣的情況很常見的,生物的產品在製程放大的過程中,比如說本來是兩公升反應槽放大10倍,可能得到的結果就不一樣,在FDA蠻多這種例子。」
梁碧惠進一步解釋:「美國Genzyme藥廠發展治療龐貝氏症的藥物Myozyme,這是一個蛋白質藥物,用在臨床試驗時的藥物是從160公升發酵槽做的,後來通過臨床試驗進行佈局全球市場的量產時,放大到2000公升發酵槽得到的成品,仔細分析後發現跟臨床試驗生產的藥物在醣化修飾有差異,FDA駁回這個量產的成品申請,藥廠後來乾脆重新做臨床試驗,變成一個新的藥物,也給新的名稱-Lumizyme。」
雖然這一次高端還沒需要重新做二期,但梁碧惠也提到:「其實一個蛋白質疫苗發展的時間需要很長,必須要做徹底的分析和確認,生產時確校要做三批,三批都要得到相同品質,若成品有問題,就要回頭仔細檢查找出問題。」
疫苗生產的不良率是很常見!國際大廠也難保證
雖然在疫苗的製造過程中,會有一定的方法檢測,被稱作「製程中控制」,即使是國際大藥廠還是沒辦法確保大量生產一定成功,「因為生物的蛋白質的生產就是這麼有趣,變成十倍的體積或是濃度不一樣就可能有不同的成品出來,這需要精密的製程中控制和成品分析。」梁碧惠說到。
但畢竟國產疫苗任何一個階段都會被高度檢視,食藥署強調:「所有疫苗於放行前,均需經過食藥署檢驗外觀、pH值、鑑別、無菌試驗、細菌內毒素、總蛋白含量、異常毒性試驗、抗原含量、效價測定等項目,完成檢驗封緘以確保品質及安全無虞,始可放行。」看來距離高端正式上路給民眾接種前,還有許多挑戰、問題需要克服。

文、王芊淩/圖、何宜庭
延伸閱讀
COVID-19/民眾可安心接種高端疫苗嗎?專家剖析國內疫苗定位
COVID-19/哪個才是「最好」的新冠疫苗?AZ、莫德納、高端該選哪一個?專家分析比較給你聽
打完兩劑疫苗後仍確診!研究剖析變種病毒造成「突破性感染」