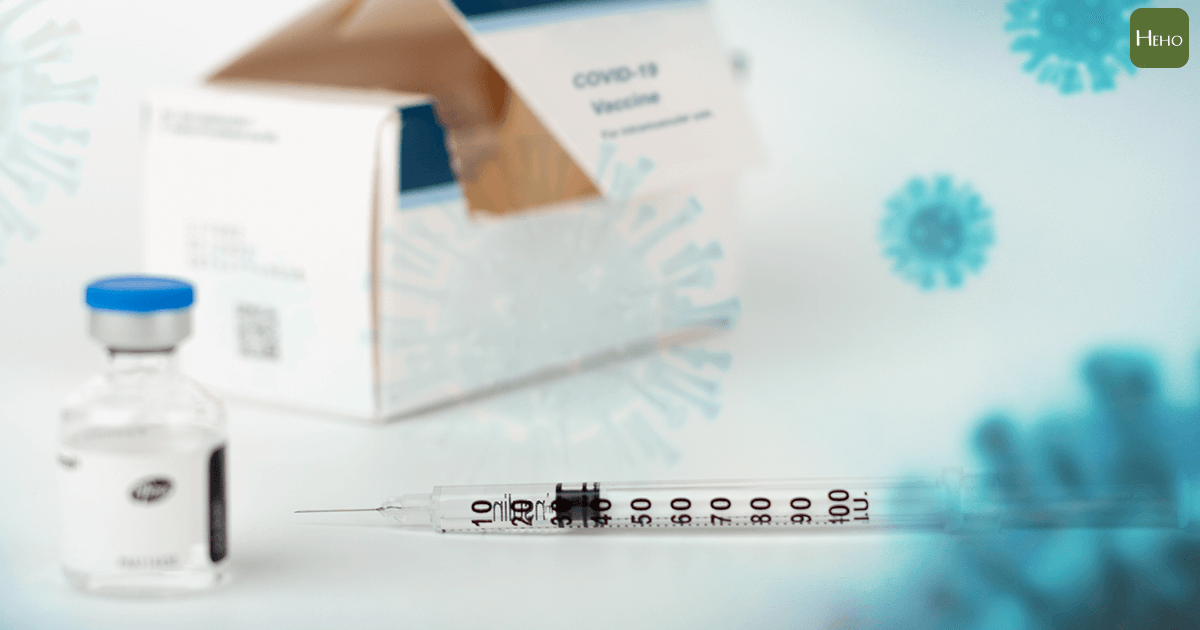
衛福部食品藥物管理署為了審查國產新冠疫苗緊急授權許可(EUA),日前公告將以英商阿斯特捷利康(AZ)藥廠的新冠疫苗做為比較基準。對於國產疫苗民眾仍十分擔憂,食藥署提出 COVID-19 疫苗緊急使用授權,擬用免疫橋接是否能真實反應出保護力?
對此,馬偕邱南昌醫師認為,疫苗的三大重點是有效性、安全性、時效性,現有疫苗緊急授權就是為了時效性。若要以其他疫苗當作對照有相當難度,要選用哪個緊急授權的疫苗來比較也需要考量的。「第三期臨床試驗仍該持續進行,但希望搶時間提供民眾有足夠的抵抗力,所以才需考量免疫橋接,以最合理的方式趕上時效性。」
邱南昌指出,疫苗臨床試驗需先評估參與試驗的人數達多少才能得知疫苗有效性,先前台灣較少新冠肺炎的案例,所以很難得知疫苗有效性。以目前台灣的感染率,可能需要約十萬人才能做出有效性的差異,而若要與其他緊急授權的疫苗比較,需要的人數據估要再多三倍。
WHO 建議各國視自身情況做免疫橋接
長庚施信如教授表示,免疫橋接標準如何制定都需進一步討論。WHO 會議上就建議各國可以視自身情況去做免疫橋接,給予各國自行判斷的決策。如果用中和抗體和AZ疫苗相比,可以得出國產疫苗的保護效果,這樣大家也會比較有信心。不過仍要提醒民眾就算打了疫苗,也要注重個人防疫。
中研院院士陳建仁指出,在台灣做 AZ 疫苗的免疫橋接測試時,須區分出自然感染產生的抗體和打疫苗產生的抗體,以免影響測試的結果。現在全球時間急迫性很重要,與過往狀況不一樣,若全球 78 億總人口需有 65% 疫苗施打率,現有緊急授權疫苗在未來一年半內是不足以應付這 55 億的人口打完兩劑,所以免疫橋接是有其必要性。
國衛院劉家齊副研究員表示,國內生產蛋白質疫苗風險相對較低,安全性應是可以比較放心。《Nature》 期刊有研究比較中和抗體效價與保護效果的關聯性,提供一個能去思考去比較的方向。我們是否能如歐美願意爭取時間制定疫苗緊急使用授權,免疫橋接對現有法規而言是很新的觀點,審慎評估並釐清法規的問題才有評估的基準。
文/林以璿 圖/林以璿
延伸閱讀:
COVID-19 / Delta 變異株肆虐全球!國內專家分析疫苗保護力影響
整理包/想打疫苗「殘劑」怎麼預約?哪些人可以打?常見疑問一次懂
整理包/一次看懂印度Delta變種病毒有什麼不同!專家分析防堵關鍵