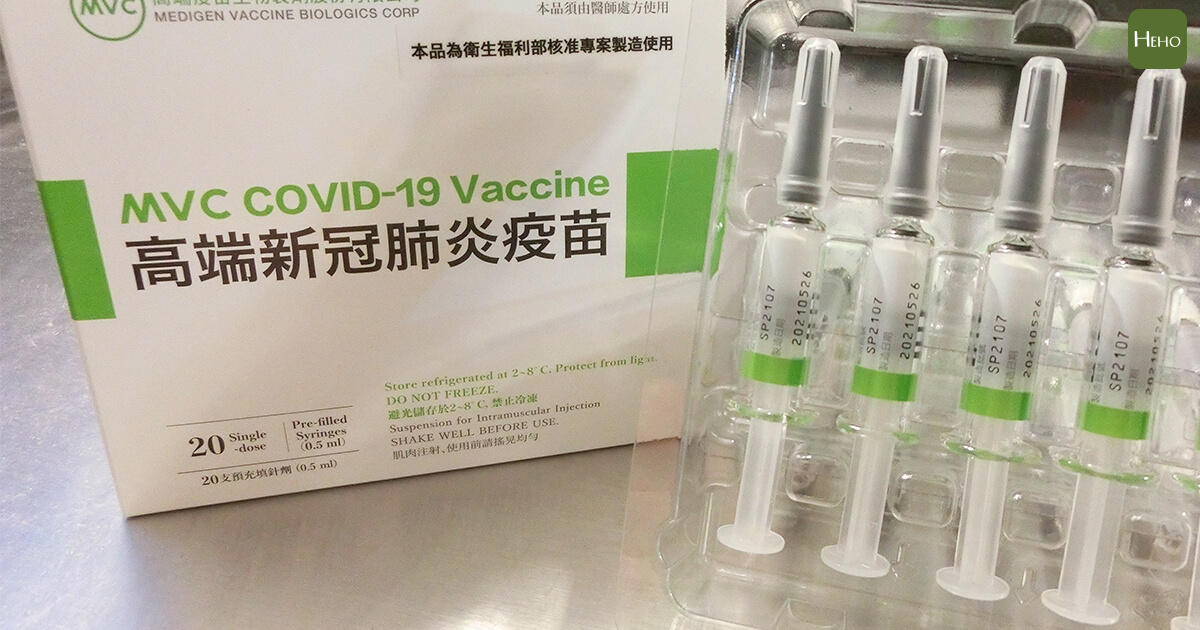
國產高端疫苗在 7 月 19 日證實通過EUA,引來外界高度討論,當時食藥署未公開專家小組審查的過程,今天突然公布專家審查會議紀錄,會議紀錄中發現多位專家提醒應該高端之後補足 T 細胞相關的反應數據,以及面對變異病毒的保護力。
參加EUA會議的專家一共有 21 人,主席不參與投票,通過 3 人、有條件通過 15 人、補件再議 1 人、不通過 1 人,但會議紀錄中全部都是以「匿名」方式表述意見。
指揮中心先前的態度認為考量疫情快速擴散,國內雖然採購及被贈與疫苗,長久下來疫苗量似乎也還不夠,自行研發疫苗應是國人的共識,但高端疫苗到底能否以免役橋接的方式就列為通過,專家以不同的觀點表述意見。
討論點一:變異病毒對高端疫苗影響
專家也提到,高端疫苗對於病毒變異株所產生之中和抗體效價降低,對於臨床保護力的影響尚未可知,應該追蹤提供抗體、保護力的持 續性、進行第三劑 booster 研究。
尤其是現在較流行的 Delta 保護力仍有疑慮,至少有 4 人提出應增加對 Delta 保護力驗證。建議未來仍須對致病力與高傳染力的變異株, 應加強研發改良型疫苗。
討論點二:中和抗體效價為疫苗保護力指標
雖然臨床試驗顯示高端疫苗中和抗體的幾何平均效價是 AZ 疫苗的 3.4 倍,專家強調:「中和抗體效價高低能否作為疫苗保護力指標,以現有數據恐不足以支持,提供更多免疫原性及疫苗保護力資料來釐清。」
尤其高端疫苗產生之中和抗體效價,「長期抗體」維持效果尚待觀察。專家點出:「而除體液性免疫外,高端疫苗以 ELISpot 進行的細胞免疫性評估資料, 仍然相當有限。」
多數專家在表示意見中都提到,不能只看中和抗體,希望高端補足有關T細胞相關的反應數據。
討論點三:疫苗未來如何使用
有專家建議:「高端疫苗沒有嚴重的不良反應發生,以長期安全性來評估,次單位蛋白疫苗有較多的使用經驗,尤其對青少年使用者,因此建議應加速執行青少年臨床試驗。」
也有專家提醒廠商仿單應對特殊族群,例如孕婦、慢性患者需要有相關資料,制定明確的使用建議。
此外,至少有 10 位專家建議,高端疫苗需補做三期臨床試驗的相關資料,也是普遍的共識,強調第三期臨床試驗應持續規劃與執行,可將第二期的延伸性試驗, 讓受試者施打第三劑,未來才能與國際接軌。
參考資料
食藥署
文、圖/王芊淩
延伸閱讀
COVID-19/民眾可安心接種高端疫苗嗎?專家剖析國內疫苗定位
COVID-19/高端疫苗通過EUA後下個考驗!疫苗為什麼會有不良率的問題?
COVID-19/我適合打高端疫苗嗎?副作用有哪些?專家黃玉成大解析