過去,癌症是眾人眼中的不治之症,即使接受了放療化療,撐過了痛苦的副作用,也只是稍微延長一點點壽命,但是CART療法的出現,讓很多人看到了希望,但它同樣面臨著很多難題。
21世紀以來,「精準」成為醫療行業追求的一大目標,無論基因檢測還是標靶治療,都顯示出了對精準的極高要求,在癌症治療領域,CART療法(嵌合抗原受體T細胞療法)亦是如此。2017 年以來,FDA先後批准兩款CAR-T細胞治療產品Kymriah和Yescarta上市,就此開啟了腫瘤免疫治療的新時代。
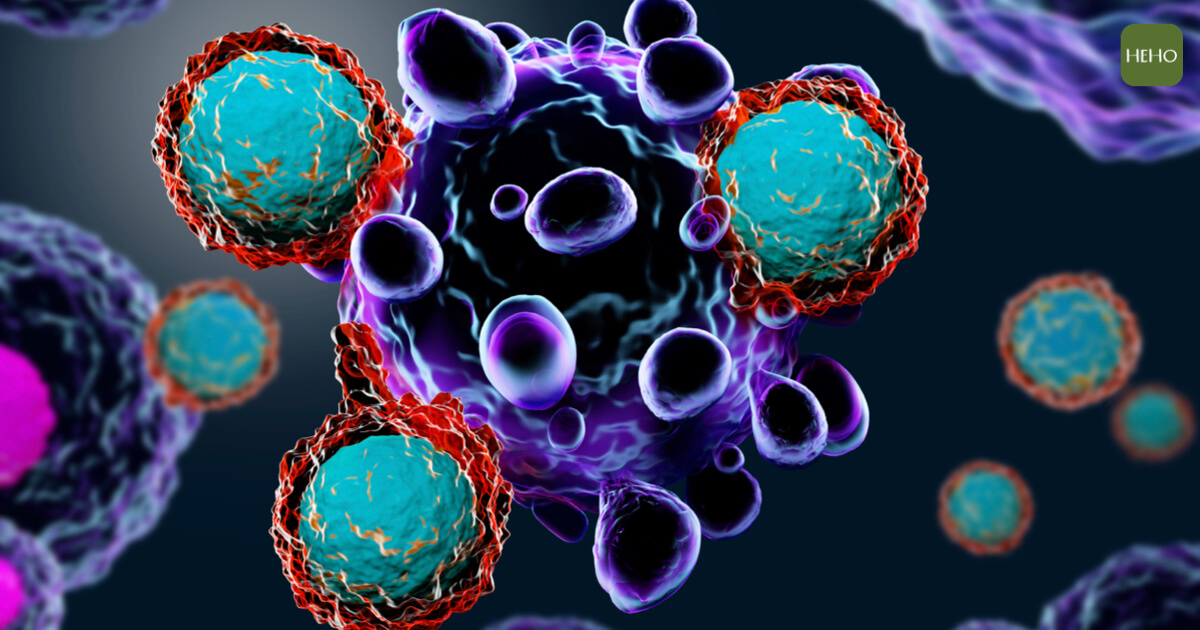
CART細胞療法是近年來發展非常迅速的細胞免疫治療技術,它將抗原抗體的高親和性,和T淋巴細胞的殺傷作用相結合,透過構建特異性嵌合抗原受體,經基因轉導使T淋巴細胞表達這種嵌合抗原受體,特異性地識別靶抗原從而殺傷靶細胞。
這聽起來似乎非常美好,靶向殺傷癌細胞,避免了對正常細胞和組織的損傷,似乎能夠完美規避目前癌症治療手段的弊端。近年來,相關治療方法已經在血液病等領域開始應用。然而,新療法不可避免的會產生一些新的問題。
細胞激素風暴(CRS)
第一代CAR-T細胞問世時,由於缺乏共刺激因子,T細胞增殖不足,細胞因子產生過少,缺乏抗腫瘤反應。於是,科學家將CAR(嵌合抗原受體)進行了改造,讓在抗腫瘤的同時,也增加細胞的體內存活時間。但是這種CAR-T細胞是把雙刃劍,改造後的增殖過度,可能引起致命性CRS,這種失控的免疫反應,往往造成器官的損傷及衰竭,進而導致休克而死亡。
現在,有學者根據之前處理T細胞治療相關CRS的經驗,提出了一套用於對CRS嚴重程度進行分級的5 級系統,並根據相應級別提供了各自的治療選擇,以使患者致命危險並發症的風險最小化,同時最大化CART治療效果。
脫靶效應
還有一種危險因素,叫「脫靶效應 」,指的是CAR-T細胞原本是要攻擊腫瘤細胞,卻錯殺了正常細胞,這是為什麼?這和CAR-T在製備過程中選擇的特異性分子很有關係。
腫瘤和正常細胞很像,就像恐怖分子通常會打扮得像老百姓,不被警察發現。如果CAR-T選擇的靶標在正常細胞上也有,正常細胞就會受到攻擊。白血病的標記分子CD19,就是一種腫瘤特異性很高的標誌,這才促成白血病領域CAR-T治療如此成功。因此在今後的CAR-T研發中,尋找特異性高的靶標是非常重要的關鍵因素。
神經毒性
除了「細胞激素風暴」外,神經毒性也是一大風險。去年 CAR-T 研究的先驅 Juno 公司,在進行 JCAR015 的 2 期臨床試驗時,先後發生多例病人因為神經毒性死亡,被 FDA 兩度叫停了臨床試驗。目前對於神經毒性沒有很好的解釋,有人說是白血病細胞侵犯到中樞神經周圍,被CAR-T攻擊後產生大量的細胞碎片,導致腦水腫。目前還沒有明確的方法可以應對。
延伸閱讀:
細胞治療特管辦法9月實行 石崇良:不只癌末 還有多項重症獲生機!
文/林以璿 圖/許嘉真