「歸巢」(homing)最早是由1983年Gallation所提出來的概念,是指循環在血液中的淋巴細胞,傾向於遷移到它們原生的淋巴結,這一回歸現象稱為「淋巴細胞的歸巢」,後來「歸巢」這一概念逐漸引申至幹細胞,是指幹細胞在多種因素的作用下,能越過血管內皮細胞至特定標靶的組織存活的過程,這樣的機制科學界一直無法了解成因,嚴重影響臨床造血幹細胞移植等相關技術的發展。而中國科學院最近破解造血幹細胞體內真正的「歸巢」過程,將帶動造血幹細胞技術的發展。
造血幹細胞的歸巢現象是?
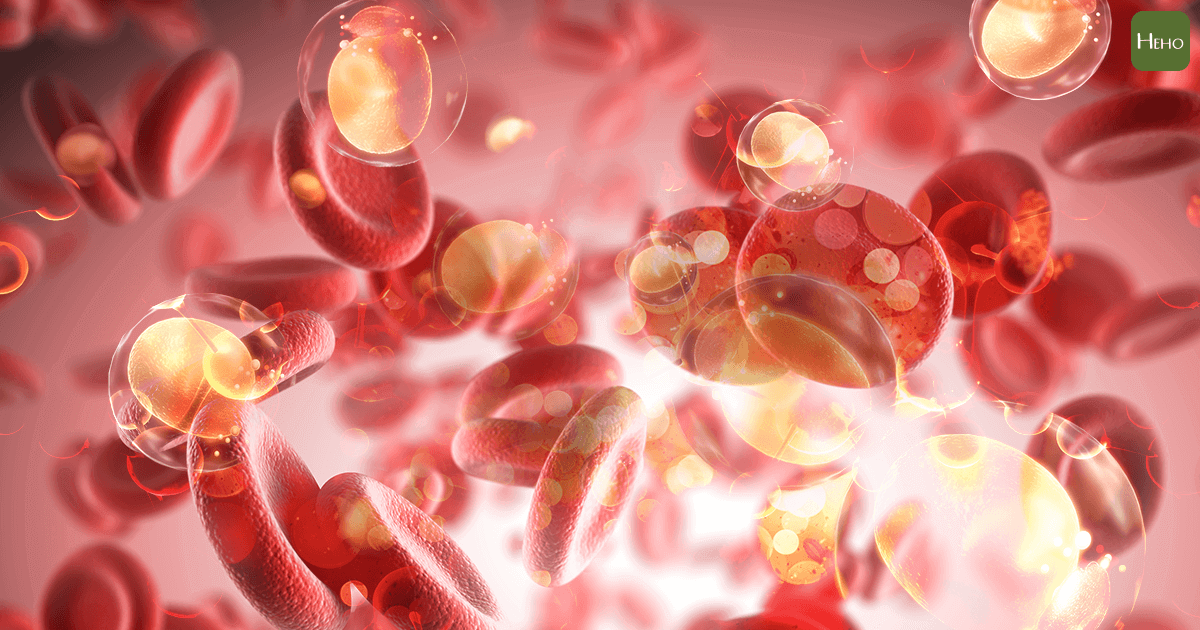
造血幹細胞是一種可以分化為各種血球的幹細胞,例如可以產生紅細胞、白細胞、血小板等人體內所有類型的血液細胞。此外,造血幹細胞能夠自我更新和向下游分化並建立整個血液系統。但在造血幹細胞建立造血系統前,會發生向造血組織的「歸巢」現象,這種現象通常是指人體循環系統中的特定細胞群會整群遷移至生物體組織或器官微環境,維持或重塑細胞群命運的生命過程。
造血幹細胞歸巢的概念形成已久,而且科學家已經應用歸巢的現象在臨床上治療血液、免疫和腫瘤等重大疾病。但因為過去觀察的工具和方法有限,所以對於歸巢現象只停留在表面。歸巢在體內生理情況下究竟如何發生,歸巢的微環境究竟是何種結構,微環境細胞又是如何幫助造血幹細胞歸巢的等一系列關鍵科學原理依然知之甚少,嚴重制約了臨床造血幹細胞移植等相關技術的發展。
「歸巢」(homing)現象就像孟母三遷
而最新的國際學術期刊《Nature》(自然),報導了中國科學院上海營養與健康研究院研究員潘巍峻顏研究團隊歷時6年,利用斑馬魚的模式生物,結合活體成像技術並透過可變色螢光蛋白標記,在高解析度共聚焦螢光顯微鏡下,建立了長時間活體觀察追蹤造血幹細胞的方法,記錄了造血幹細胞從誕生到歸巢的全程,並透過影像分析發現造血幹細胞歸巢的熱區和時間空間的分布規律,並將數據結合精細成像和三維重構技術,還原了體內造血幹細胞歸巢微環境的獨特微血管結構。
在研究過程中,研究團隊還意外發現了一種全新的微環境細胞,並命名為「先導細胞」,屬於從未被定義過的巨噬細胞新亞型,存在於「歸巢熱區」附近,它們可以識別進入造血組織的造血幹細胞,並引導造血幹細胞進入特定的血管結構中,導致造血幹細胞的歸巢現象。研究團隊的主持人潘巍峻表示,歸巢現象就像孟母三遷,在身體健康的狀態下,造血幹細胞好像裝有偵測體內最佳環境位置的GPS。
研究結果除了解答體內造血幹細胞,怎麼發生歸巢現象的問體外,還發現了引導歸巢作用的先導細胞,對於提高造血細胞的移植轉化效率的提出了新理論,更可協助臨床上血液、免疫和腫瘤等重大疾病的治療。
延伸閱讀
再生醫學(21):再生醫學培養迷你食道救助先天食道缺損幼童!
文/黃聖筑 圖/許嘉真